Definicja i zastosowanie markera białkowego
Marker białkowy to mieszanina białek o znanej masie cząsteczkowej, która służy jako „linijka” do wskazania wielkości prążków białkowych.
W procesie Western Blot marker masy cząsteczkowej przypomina śrubę, chociaż jest to małe ogniwo, jednak jest to tak mały szczegół, który ma znaczący wpływ na wyniki eksperymentu. Rola markera służy głównie do wskazania masy cząsteczkowej prążków białkowych odpowiadającej wielkości masy cząsteczkowej i tylko wtedy, gdy standardowa ilość jest dokładna i poprawna, wyniki eksperymentów są przekonujące, oprócz markera białkowego pokazuje również, czy membrana jest transfekowana, czy nie. Poza tym pokazuje także, czy transfer przez błonę przebiegł pomyślnie, czy nie, oraz stopień elektroforezy białka na żelu itp. Dlatego też dobór odpowiedniego markera białkowego jest także jednym z niezbędnych warunków powodzenia eksperymentów Western Blot.
Klasyfikacja markerów białkowych
Ogólnie rzecz biorąc, najczęściej stosowane markery białkowe dzielą się na niezabarwione markery białkowe i wstępnie wybarwione markery białkowe.
Jest to premiks kilku białek o znanej masie cząsteczkowej i oczyszczonych, co jest wygodne do porównywania białek o różnej wielkości. Marker niebarwiony nie jest tak dobry jak Marker wstępnie wybarwiony, ponieważ jest całkowicie niewidoczny podczas elektroforezy i można go wskazać dopiero po wybarwieniu białek pod koniec elektroforezy i nie może być używany jako punkt odniesienia w procesie eksperymentalnym, co należy do typu „spostrzeżeń z perspektywy czasu”. Ponieważ jednak białku nie towarzyszy cząsteczka barwnika ani cząsteczka markera, pokazany rozmiar jest dokładnie taki sam, jak pierwotny rozmiar białka, więc jest dokładniejszy i umożliwia dokładniejsze określenie wielkości białka.


Wstępnie zmieszany Marker ma zwykle kilka pasm, które podwajają stężenie w celach informacyjnych, ponieważ im więcej pasm jest zmieszanych, tym trudniej jest zapamiętać, kto wie, który to ten! Trudno liczyć, dopóki oczy się nie zamazują. Kiedy więc zobaczysz te szczególnie skoncentrowane, paski znaczników zapamiętają, gdzie się znajdują. Pamiętaj jednak, że mniejsze pasma zwykle nie są tak łatwe do zauważenia. Jeśli chodzi o selekcję, oczywiście najlepiej jest wybrać co najmniej jedno z prążków, które jest podobne pod względem wielkości do docelowego białka, im bliżej, tym lepiej.
Wstępnie barwiony marker białkowy to oczyszczone białka zmieszane razem poprzez kowalencyjne sprzęganie z barwnikiem, co można bezpośrednio zaobserwować podczas elektroforezy lub transferu membranowego.
Wstępnie wybarwione markery białkowe są wygodne w naszych eksperymentach. Ten standard masy cząsteczkowej białka może pomóc nam monitorować elektroforezę i oszacować ruchliwość podczas i po elektroforezie, a także po transferze membrany - na przykład, jeśli wiadomo, że optymalna strefa rozdzielczości dla elektroforezy pionowej wynosi około 2/3 drogi przez żel, przy użyciu wstępnie zabarwionego markera można np. Wiadomo, że optymalna strefa rozdzielczości elektroforezy pionowej wynosi około 2/3 żelu, jeśli używasz wstępnie zabarwionego markera, możesz przewidzieć, kiedy docelowe białko wejdzie w strefę optymalnej rozdzielczości i zatrzymać elektroforezę, aby uzyskać optymalny efekt rozdzielczości; możesz także przerwać elektroforezę w odpowiednim czasie, jeśli zaobserwujesz nieprawidłowości w elektroforezie Markera; ponadto można zaobserwować, czy białko jest całkowicie przeniesione na membranę po przeniesieniu membrany w badaniu Western Blot i można oznaczyć masę cząsteczkową białka na membranie, dlatego wiele laboratoriów przyciąga do zakupu wstępnie wybarwionego standardu białka.
Warto zaznaczyć, że wstępnie wybarwiony marker białkowy jest kowalencyjnie związany z barwnikiem, zatem charakterystyka migracji może ulec zmianie przy elektroforezie w różnych warunkach buforowych, co może prowadzić do pewnych odchyleń, przez co nie nadaje się do precyzyjnej lokalizacji białek – jednak w większości przypadków prążki na markerze mogą nie być identyczne z białkiem docelowym, a wyniki, jakie otrzymamy, będą dokładnie takie same, jak białka docelowego. Jednak w większości przypadków prążki Markera mogą nie być dokładnie takie same jak nasze docelowe białko, a to, co otrzymujemy, to tylko rozmiar odniesienia w stosunku do wskazania Markera, a ostatecznie potrzebujemy Westerna, aby go scharakteryzować, więc jeśli nie musimy rozróżniać prążków o podobnych rozmiarach, wstępnie wybarwiony Marker jest nadal bardzo przydatny i można go również stosować w połączeniu z niezabarwionym standardem białka.
Klasyfikacja wstępnie barwionego markera białkowego
Wstępnie barwiony Marker białkowy dzieli się na: monochromatyczny wstępnie barwiony i wielobarwny wstępnie barwiony, monochromatyczny wstępnie barwiony Marker białkowy zazwyczaj wykorzystuje niektóre prążki do podwojenia stężenia niektórych prążków, aby pogłębić grubość niektórych prążków, aby zasugerować wielkość ich wielkości, abyśmy mogli szybko zapamiętać i rozróżnić wielkość poszczególnych prążków. Kolorowe markery białkowe wyróżniają się różnymi kolorami, co jest jeszcze bardziej rozpoznawalne. Co więcej, jeśli w nudnym eksperymencie z elektroforezą wyjdzie kolorowy tęczowy Marker, nastrój będzie w tym czasie weselszy!
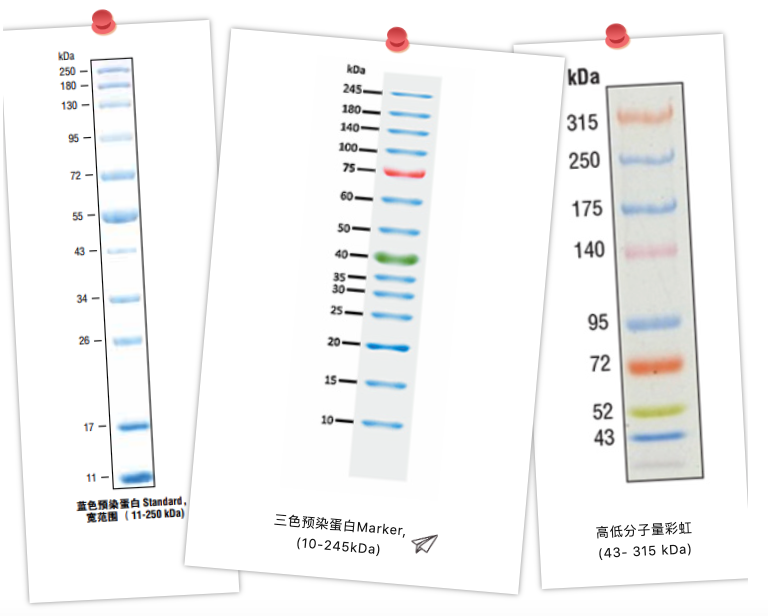
Oprócz powyższego na rynku dostępnych jest kilka innych rodzajów markerów białkowych: fluorescencyjne markery białkowe, markery biotynylowane, rozwinięte markery białkowe itp.
Ponadto markery białkowe dzieli się na kategorie o wysokiej masie cząsteczkowej, o niskiej masie cząsteczkowej i o szerokiej masie cząsteczkowej, zgodnie z zakresem masy cząsteczkowej. Markery o wysokim zakresie mas cząsteczkowych są często stosowane w przypadku białek o dużej masie cząsteczkowej, podczas gdy markery o niskim zakresie mas cząsteczkowych są często używane w przypadku małych białek, a nawet niektórych peptydów. jeśli rozważasz całe laboratorium, wybierz markery o szerokiej masie cząsteczkowej z bardziej równomiernym rozkładem pasm, aby można było łatwo ocenić białka bez względu na to, w którym przedziale się znajdują.
Niektóre problemy z Markerem
Na przykład instrukcja obsługi wymienia 7 pasm, w rzeczywistości wyczerpanie się 6 pasm jest normalnym zjawiskiem, może się zdarzyć, że czas działania nie będzie wystarczający, jeśli twoje białko nie jest bardzo małe, możesz poczekać, aż front błękitu bromofenolowego wyczerpie się z żelu, zanim wyłączysz aparat do elektroforezy, tak aby powinno być 7 pasm. Czasami będzie 5 prążków, ale o ile górne i dolne dwa prążki docelowego białka mogą zostać wyczerpane, nie musi to być 7 prążków.
Po pierwsze, żel nie jest prasowany
Po drugie, płynność kleju na brzegu płytki i w środku kleju może być różna, nie ma na to sposobu, lepkością i napięciem powierzchniowym. Jeżeli powyższe zjawisko nie jest w stanie rozwiązać różnymi metodami, doradca osobisty, aby zmienić kanał w próbce, wybrać tor w pobliżu środka toru do pływania, aby pobiegać.
Efekt krawędziowy, na krawędzi dwóch pasów próbki będzie taki. Możesz spróbować wolniejszej szybkości elektroforezy......
Albo klej nie jest dobrze dociśnięty po przygotowaniu, klej nie jest dobrze przygotowany, albo napięcie elektroforezy jest zbyt wysokie, siła elektroosmotyczna jest duża, albo płytka szklana nie jest dobrze zaciśnięta podczas elektroforezy, a wewnętrzny roztwór do elektroforezy wycieka, sprawdź je jeden po drugim.
Przyczyna 1: Objętość próbki jest za duża, należy zmniejszyć objętość próbki.
Środek zaradczy: Objętość próbki powinna być elastycznie kontrolowana w zależności od stężenia próbki i grubości żelu. Ogólnie objętość próbki wynosi 10-15 µl (tj. 2-10 µg białka). Jeśli próbka jest bardzo rozcieńczona, objętość próbki może osiągnąć 100 μl.
Przyczyna 2: Niecałkowite rozpuszczenie próbki.
Środki zaradcze:
(1) Próbka powinna być całkowicie rozpuszczona: przechowuj wszystkie rodzaje próbek białek, a znacznik można całkowicie rozpuścić przed pobraniem próbki. Lepiej jest odwirować próbkę przed pobraniem próbki i usunąć cząstki, których nie można rozpuścić.
(2) Można dodać roztwór do rozpuszczania próbki zgodnie z wymaganiami zestawów białkowych do oznaczania wzorców masy cząsteczkowej; jeśli próbki standardowe i nieznane są konfigurowane samodzielnie, należy zastosować roztwór do rozpuszczania próbki o stężeniu 0,5–1,0 mg/l. Po rozpuszczeniu przenieść go do rurki Ep, założyć zakrętkę (można dodać klips na zakrętce), a następnie podgrzewać w łaźni wodnej o temperaturze 110 stopni Celsjusza przez 3 minuty (można wywiercić kilka okrągłych otworów o tej samej średnicy co rurka Ep w cienkiej płycie styropianowej i rurkę Ep odłożyć do momentu, aż krawędź zakrętki nie będzie już mogła dalej opadać, a następnie nałożyć cienką płytkę styropianową, która odsłania większość korpusu Rurka Ep we wrzącej łaźni wodnej, a cienka płyta styropianowa unosi się naturalnie we wrzącej łaźni wodnej. Cienki arkusz styropianu naturalnie unosi się na powierzchni wrzącej wody, ułatwiając dostęp i podgrzewanie oraz unikając rozpryskiwania wrzącej wody.
Partię probówek Ep można umieścić we wrzącej łaźni wodnej na różny czas. (Nie wrzucaj probówek Ep do wrzącej łaźni wodnej, pokrywki można zmyć), a następnie schłódź w temperaturze pokojowej przed użyciem. Jeżeli próbka nie jest używana przez dłuższy okres czasu, należy ją przechowywać w lodówce w temperaturze -20 stopni Celsjusza, a w razie potrzeby podgrzać próbkę we wrzącej wodzie o temperaturze 110 stopni Celsjusza przez 3 minuty w temperaturze pokojowej i ostudzić przed wyjęciem do użycia, a następnie nałożyć próbkę w celu usunięcia niestabilnych agregatów z białek próbki.
(3) Zmienić roztwór buforu próbki tak, aby próbka mogła zostać całkowicie rozpuszczona, a ilość SDS powinna być wystarczająca.
Powód: pasma SDS są połączone elektroforetycznie z sąsiadującymi białkami. Oprócz nadmiernego pobierania próbek i niecałkowitego rozpuszczenia próbki, wyciek żelu z dołków próbki może powodować poszerzenie pasm elektroforetycznych. Wyciek jest często spowodowany pęknięciami pomiędzy żelem a płytką szklaną. Środki zaradcze: W tym momencie żel można jedynie ponownie przygotować, należy zachować ostrożność przy wyrywaniu grzebienia, aż do uzyskania spójności żelu, prędkość nie powinna być zbyt duża, kierunek wyrywania powinien być prostopadły do powierzchni żelu; aby uniknąć pęknięć pomiędzy płytką szklaną po obu stronach żelu a żelem, w procesie przygotowania żelu nie należy ściskać płytki szklanej po obu stronach żelu.



