Proteinmarkör Definition och användning
Protein Marker är en blandning av proteiner med känd molekylvikt, som används som en 'linjal' för att indikera storleken på proteinband.
I processen med Western Blot är molekylviktsmarkören som en skruv, även om det är en liten länk, men det är en så liten detalj som har en betydande effekt på experimentresultaten. Markörens roll används huvudsakligen för att indikera molekylvikten för proteinbanden som motsvarar storleken på molekylvikten, och endast om standardmängden exakt och korrekt, resultaten av de transfekterade membranexperimenten också visar huruvida de transfekterade membranexperimenten är övertygande eller inte. Dessutom visar den också om membranöverföringen är framgångsrik eller inte, och graden av elektrofores av proteinet på gelén, etc. Därför är valet av rätt proteinmarkör också en av de nödvändiga förutsättningarna för framgång med Western Blot-experiment.
Klassificering av proteinmarkörer
I allmänhet är de vanligast använda proteinmarkörerna kategoriserade i icke-förfärgade proteinmarkörer och förfärgade proteinmarkörer.
Det är en förblandning av flera proteiner med känd molekylvikt och renade, vilket är bekvämt för jämförelse av proteiner av olika storlekar. Non-pre-stained Marker är inte lika bra som pre-stained Marker eftersom den är helt osynlig under elektrofores, och kan endast indikeras efter proteinfärgning i slutet av elektrofores, och kan inte användas som referens i den experimentella processen, som hör till typen av 'eftersyn'. Men eftersom proteinet inte åtföljs av en färgämnesmolekyl eller en markörmolekyl, är storleken som visas exakt den ursprungliga storleken på proteinet, så det är mer exakt och kan exakt bestämma storleken på proteinet.


Pre-mixed Marker brukar ha några få band som fördubblar koncentrationen som en indikation, för ju fler band som blandas desto värre är det att komma ihåg, vem vet vilket är det! Det är svårt att räkna tills dina ögon är suddiga. Så när du ser de särskilt koncentrerade kommer markörbanden ihåg var de är. Kom dock ihåg att de mindre banden vanligtvis inte är lika lätta att se. När det gäller urval är det förstås bäst att välja minst ett av banden som är lika i storlek som ditt målprotein, ju närmare desto bättre.
Förfärgad proteinmarkör är några renade proteiner blandade genom kovalent koppling med ett färgämne, som kan observeras direkt under elektrofores eller membranöverföring.
Förfärgade proteinmarkörer är bekväma för våra experiment. Denna proteinmolekylviktsstandard kan hjälpa oss att övervaka elektrofores och uppskatta rörlighet under och efter elektrofores, såväl som efter membranöverföring - till exempel, om det är känt att den optimala upplösningszonen för vertikal elektrofores är cirka 2/3 av vägen genom gelén, med hjälp av en förfärgad markör är det möjligt att Till exempel är det känt att om du använder den optimala upplösningszonen för en vertikal,/3 pre-stained Marker, du kan förutsäga när målproteinet går in i den optimala upplösningszonen och stoppa elektroforesen för att få den optimala upplösningseffekten; du kan också avsluta elektroforesen i tid om du observerar en abnormitet i elektroforesen av Marker; dessutom kan man observera om proteinet överförs helt till membranet efter överföringen av membran i Western Blot och man kan märka proteinets molekylvikt på membranet, varför det lockar många laboratorier att köpa den förfärgade proteinstandarden.
Det är värt att notera att den förfärgade proteinmarkören är kovalent kopplad med färgämnet, så migrationsegenskaperna kan ändras vid elektrofores under olika buffertförhållanden, vilket kan leda till vissa avvikelser, så det är inte lämpligt för exakt lokalisering av proteiner - men i de flesta fall kanske banden på markören inte är identiska med målproteinet, och samma resultat som målproteinet är bara samma resultat som målproteinet. Men i de flesta fall kanske markörbanden inte är exakt samma som vårt målprotein, och det vi får är bara en referensstorlek i förhållande till markörindikationen, och i slutändan behöver vi Western för att karakterisera det, så om vi inte behöver skilja mellan band av liknande storlekar är den förfärgade markören fortfarande mycket användbar, och den kan också användas i kombination med det icke-sammansatta proteinet.
Klassificering av förfärgad proteinmarkör
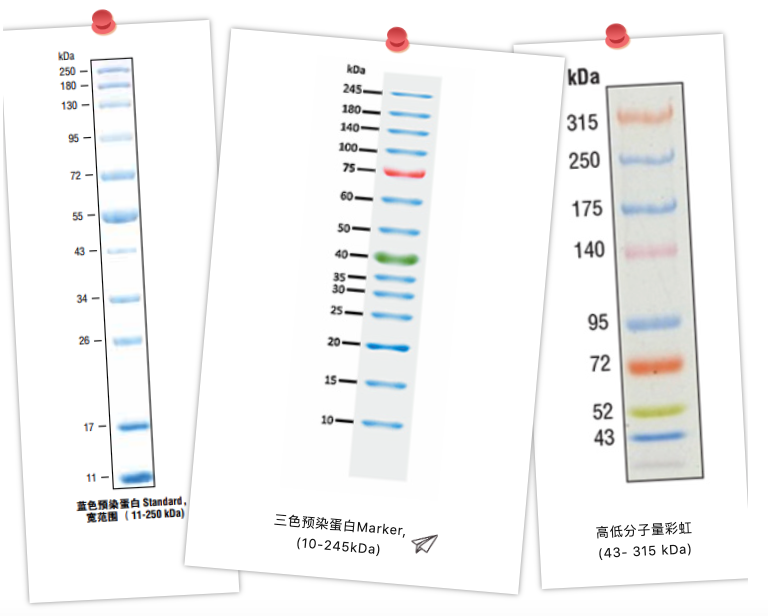
Förfärgad proteinmarkör är indelad i: monokrom förfärgad och flerfärgad förfärgad, monokrom förfärgad proteinmarkör kommer vanligtvis att använda några av banden för att fördubbla koncentrationen av vissa band för att fördjupa tjockleken på vissa band för att föreslå storleken på deras storlek, så att vi snabbt kan memorera och skilja mellan storleken på de enskilda banden. Färgproteinmarkörer kännetecknas av olika färger, vilket är ännu mer igenkännbart. Dessutom, om en färgglad regnbågsmarkör kommer ut i ett tråkigt elektroforesexperiment, kommer stämningen att vara gladare vid den här tiden!
Utöver ovanstående finns det några andra typer av proteinmarkörer på marknaden: fluorescerande proteinmarkörer, biotinylerade markörer, utvecklade proteinmarkörer, etc....
Dessutom kategoriseras proteinmarkörer i hög molekylvikt, låg molekylvikt och bred molekylvikt enligt molekylviktsintervall. Markörer med hög molekylvikt används ofta för proteiner med stor molekylvikt, medan markörer med låg molekylvikt ofta används för små proteiner eller till och med vissa peptider. om du tänker på hela laboratoriet, välj breda molekylviktsmarkörer med mer enhetlig bandfördelning, så att dina proteiner lätt kan bedömas oavsett vilket intervall de befinner sig i.
Vissa problem med Marker
Till exempel listar bruksanvisningen 7 band, i själva verket är det normalt att ta slut på 6 band, det kan vara så att körtiden inte räcker till, om ditt protein inte är väldigt litet kan du vänta tills den bromfenolblå fronten rinner ur gelén innan du stänger av elektroforesapparaten, så att du ska kunna ha 7 band. Ibland kommer det att finnas 5 band, men så länge de två övre och nedre två banden av ditt målprotein kan ta slut, behöver det inte vara 7 band.
För det första pressas inte gelen
För det andra kan limmets flytbarhet vid kanten av plattan och mitten av limmet vara olika, det finns inget sätt att göra detta med viskositeten och ytspänningen. Om en mängd olika metoder inte kan lösa ovanstående fenomen, personlig rådgivning maker för att ändra en kanal på provet, välj ett körfält nära mitten av simbanan för att springa.
Kanteffekt, vid kanten av provets två körfält kommer att vara så här. Du kan prova långsammare elektroforeshastighet ......
Antingen är limmet inte väl pressat när det förbereds, limmet är inte väl förberett eller så är elektroforesspänningen för hög, den elektroosmotiska kraften är stark eller så är glasplattan inte väl fastklämd under elektrofores och den inre elektroforeslösningen läcker, kontrollera dem en efter en.
Orsak 1: Provvolymen är för stor, provvolymen bör minskas.
Motåtgärd: Provvolymen bör styras flexibelt i enlighet med provkoncentrationen och geltjockleken. I allmänhet är provvolymen 10-15μL (dvs. 2-10μg protein). Om provet är mycket utspätt kan provvolymen nå 100μL.
Orsak 2: Ofullständig upplösning av provet.
Motåtgärder:
(1) Provet bör vara helt upplöst: behåll alla typer av proteinprover och Marker kan lösas helt före provtagning, det är bättre att centrifugera provet före provtagning och ta bort partiklarna som inte kan lösas upp.
(2) Provlösningslösning kan tillsättas enligt kraven för proteinkit för molekylviktsstandarder; om standardprov och okända prover är självkonfigurerade, följ 0,5-1,0 mg/L provlösningslösning. Efter upplösning, för över den till Ep-röret, sätt på locket (du kan lägga till en klämma vid locket) och värm det sedan i ett vattenbad vid 110 grader Celsius i 3 minuter (du kan borra flera runda hål med samma diameter som Ep-röret i den tunna frigolitplattan, och Ep-röret läggs ner tills kanten på locket hålls nere, och sedan stoppas ev. exponerar det mesta av kroppen på Ep-röret, i det kokande vattenbadet, och den tunna frigolitplattan flyter naturligt i det kokande vattenbadet.
En sats av Ep-rör kan placeras i det kokande vattenbadet för olika tider. (Kasta inte Ep-rören i det kokande vattenbadet, locken kan tvättas av) och kyl sedan i rumstemperatur för användning. Om provet inte används under en längre tid, förvara provet i ett kylskåp vid -20 grader Celsius, och vid behov värm provet i kokande vatten vid 110 grader Celsius i 3 minuter vid rumstemperatur och kyl det innan du tar bort det för användning och applicerar sedan provet för att avlägsna de substabila aggregaten i provproteinerna.
(3) Byt ut provbuffertlösningen så att provet kan lösas upp helt och mängden SDS bör vara tillräcklig.
Anledning: SDS-band är elektroforetiskt kopplade till närliggande proteiner. Förutom överprovtagning och ofullständig upplösning av provet kan läckage av gelens provbrunnar göra att de elektroforetiska banden vidgas. Läckaget orsakas ofta av sprickor mellan gelén och glasplattan. Motåtgärder: Vid denna tidpunkt kan gelén bara förberedas på nytt, kammen bör vara försiktig när du drar upp gelens sammanhållning är klar, hastigheten bör inte vara för hög, riktningen för att dra upp bör vara vinkelrät mot ytan av gelen; För att undvika sprickor mellan glasplattan på båda sidorna av gelén och gelén, kläm inte glasplattan på båda sidorna av gelén under gelberedningen.



