Definizione e utilizzo dei marcatori proteici
Il Protein Marker è una miscela di proteine di peso molecolare noto, che viene utilizzata come un 'righello' per indicare la dimensione delle bande proteiche.
Nel processo di Western Blot, il marcatore del peso molecolare è come una vite, anche se è un piccolo anello, tuttavia, è un dettaglio così piccolo che ha un effetto significativo sui risultati sperimentali. Il ruolo del marcatore viene utilizzato principalmente per indicare il peso molecolare delle bande proteiche corrispondenti alla dimensione del peso molecolare, e solo se la quantità standard è accurata e corretta, i risultati degli esperimenti sono convincenti, oltre al marcatore proteico mostra anche se la membrana è transfettata o meno. Inoltre, mostra anche se il trasferimento sulla membrana ha avuto successo o meno, il grado di elettroforesi della proteina sul gel, ecc. Pertanto, la scelta del giusto marcatore proteico è anche una delle condizioni necessarie per il successo degli esperimenti Western Blot.
Classificazione dei marcatori proteici
In generale, i marcatori proteici più comunemente utilizzati sono classificati in marcatori proteici non precolorati e marcatori proteici precolorati.
È una premiscela di diverse proteine di peso molecolare noto e purificate, utile per il confronto di proteine di diverse dimensioni. Il marcatore non precolorato non è buono quanto il marcatore precolorato perché è completamente invisibile durante l'elettroforesi e può essere indicato solo dopo la colorazione delle proteine al termine dell'elettroforesi e non può essere utilizzato come riferimento nel processo sperimentale, che appartiene al tipo di 'senno di poi'. Tuttavia, poiché la proteina non è accompagnata da una molecola colorante o da una molecola marcatore, la dimensione mostrata è esattamente la dimensione originale della proteina, quindi è più accurata e può determinare con precisione la dimensione della proteina.


Il Marker premiscelato solitamente ha alcune bande che raddoppiano la concentrazione come indicazione, perché più bande vengono mescolate peggio è da ricordare, chissà quale è quello! È difficile contare finché i tuoi occhi non sono offuscati. Quindi quando vedi quelli particolarmente concentrati le bande marcatrici ricorderanno dove si trovano. Ricorda però che le bande più piccole di solito non sono così facili da vedere. In termini di selezione, ovviamente, è meglio scegliere almeno una delle bande di dimensioni simili alla proteina target, più vicina è, meglio è.
Il marcatore proteico precolorato è costituito da alcune proteine purificate mescolate insieme mediante accoppiamento covalente con un colorante, che può essere osservato direttamente durante l'elettroforesi o il trasferimento sulla membrana.
I marcatori proteici precolorati sono utili per i nostri esperimenti. Questo standard di peso molecolare delle proteine può aiutarci a monitorare l'elettroforesi e stimare la mobilità durante e dopo l'elettroforesi, nonché dopo il trasferimento sulla membrana - ad esempio, se è noto che la zona di risoluzione ottimale per l'elettroforesi verticale è circa 2/3 del percorso attraverso il gel, utilizzando un marcatore precolorato è possibile Ad esempio, è noto che la zona di risoluzione ottimale dell'elettroforesi verticale è circa 2/3 del gel, se si utilizza un marcatore precolorato, è possibile prevedere quando la proteina bersaglio entra nella zona di risoluzione ottimale e interrompe l'elettroforesi per ottenere l'effetto di risoluzione ottimale; è anche possibile interrompere in tempo l'elettroforesi se si osserva un'anomalia nell'elettroforesi del Marker; inoltre, è possibile osservare se la proteina viene trasferita completamente alla membrana dopo il trasferimento della membrana nel Western Blot ed è possibile etichettare il peso molecolare della proteina sulla membrana, motivo per cui molti laboratori acquistano lo standard proteico precolorato.
Vale la pena notare che il marcatore proteico precolorato è accoppiato in modo covalente con il colorante, quindi le caratteristiche di migrazione possono cambiare quando elettroforizzato in diverse condizioni tampone, il che può portare ad alcune deviazioni, quindi non è adatto per una localizzazione precisa delle proteine - tuttavia, nella maggior parte dei casi, le bande sul marcatore potrebbero non essere identiche alla proteina target e i risultati che otteniamo sono proprio gli stessi della proteina target. Tuttavia, nella maggior parte dei casi, le bande del marcatore potrebbero non essere esattamente le stesse della nostra proteina target e ciò che otteniamo è solo una dimensione di riferimento relativa all'indicazione del marcatore e, alla fine, abbiamo bisogno di Western per caratterizzarla, quindi se non abbiamo bisogno di distinguere tra bande di dimensioni simili, il marcatore precolorato è comunque molto utile e può essere utilizzato anche insieme allo standard proteico non colorato.
Classificazione dei marcatori proteici preservati
Il marcatore proteico precolorato è suddiviso in: marcatore proteico monocromatico precolorato e precolorato multicolore, marcatore proteico monocromatico precolorato solitamente utilizza alcune bande per raddoppiare la concentrazione di determinate bande per approfondire lo spessore di alcune bande per suggerire la dimensione della loro dimensione, in modo da poter memorizzare e differenziare rapidamente le dimensioni delle singole bande. I marcatori proteici colorati si distinguono per diversi colori, il che li rende ancora più riconoscibili. Inoltre, se durante un noioso esperimento di elettroforesi esce un pennarello arcobaleno colorato, l'atmosfera sarà più felice in questo momento!
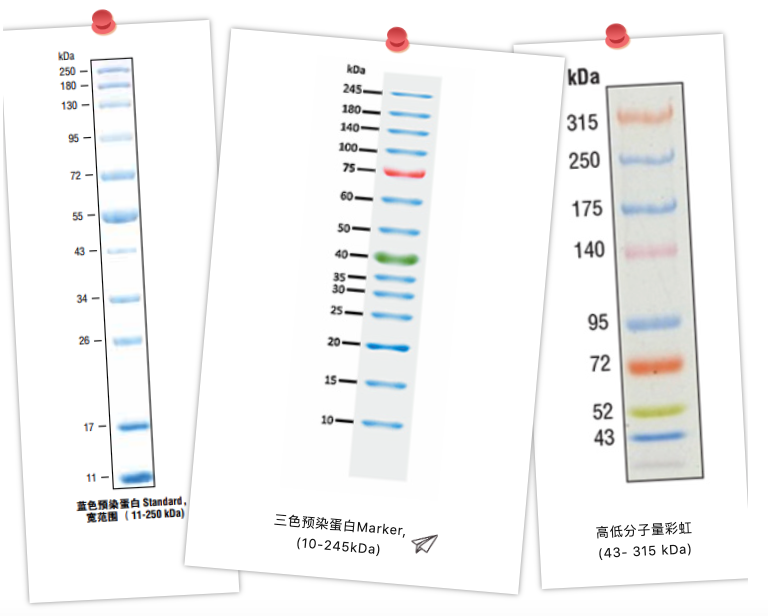
Oltre a quanto sopra, ci sono altri tipi di marcatori proteici sul mercato: marcatori proteici fluorescenti, marcatori biotinilati, marcatori proteici sviluppati, ecc....
Inoltre, i marcatori proteici sono classificati in ad alto peso molecolare, a basso peso molecolare e ad ampio peso molecolare in base all'intervallo di peso molecolare. I marcatori con intervallo di peso molecolare elevato vengono spesso utilizzati per proteine di grande peso molecolare, mentre i marcatori con intervallo di peso molecolare piccolo vengono spesso utilizzati per proteine di piccole dimensioni o anche per alcuni peptidi. se consideri l'intero laboratorio, scegli marcatori ad ampio peso molecolare con una distribuzione delle bande più uniforme, in modo che le tue proteine possano essere facilmente giudicate indipendentemente dall'intervallo in cui si trovano.
Alcuni problemi con Marker
Ad esempio il manuale di istruzioni elenca 7 bande, infatti è normale esaurire 6 bande, può darsi che il tempo di esecuzione non sia sufficiente, se le vostre proteine non sono molto piccole, potete aspettare che il fronte blu di bromofenolo finisca dal gel prima di spegnere l'apparecchio per l'elettroforesi, quindi dovreste riuscire ad avere 7 bande. A volte ci saranno 5 bande, ma finché le due bande superiore e inferiore della proteina target possono essere esaurite, non è necessario che siano 7 bande.
Innanzitutto, il gel non viene pressato
In secondo luogo, la fluidità della colla sul bordo della piastra e al centro della colla può essere diversa, non c'è modo di farlo, a causa della viscosità e della tensione superficiale. Se una varietà di metodi non è in grado di risolvere il fenomeno di cui sopra, il consulente personale consiglia di cambiare un canale sul campione, scegliere una corsia vicino al centro della corsia di nuoto per eseguire una corsa.
L'effetto Edge, sul bordo delle due corsie del campione, sarà così. Puoi provare ad abbassare la velocità dell'elettroforesi...
La colla non è ben pressata quando viene preparata, la colla non è ben preparata, oppure la tensione dell'elettroforesi è troppo alta, la forza elettroosmotica è forte, oppure la lastra di vetro non è ben fissata durante l'elettroforesi e la soluzione interna dell'elettroforesi perde, controllarli uno per uno.
Causa 1: il volume del campione è eccessivo, è necessario ridurlo.
Contromisura: il volume del campione deve essere controllato in modo flessibile in base alla concentrazione del campione e allo spessore del gel. Generalmente, il volume del campione è di 10-15μL (ovvero 2-10μg di proteine). Se il campione è molto diluito, il volume del campione può raggiungere 100μL.
Causa 2: dissoluzione incompleta del campione.
Contromisure:
(1) Il campione deve essere completamente disciolto: conservare tutti i tipi di campioni proteici e il marcatore può essere completamente disciolto prima del campionamento, è meglio centrifugare il campione prima del campionamento e rimuovere le particelle che non possono essere dissolte.
(2) La soluzione di dissoluzione del campione può essere aggiunta in base ai requisiti dei kit di proteine per gli standard di peso molecolare; se i campioni standard e sconosciuti sono autoconfigurati, seguire una soluzione di dissoluzione del campione da 0,5-1,0 mg/l. Dopo la dissoluzione, trasferiscilo nella provetta Ep, metti il tappo (puoi aggiungere una clip sul tappo) e poi scaldalo a bagnomaria a 110 gradi Celsius per 3 minuti (puoi praticare diversi fori rotondi con lo stesso diametro del tubo Ep nella sottile piastra di polistirolo, e il tubo Ep viene posizionato finché il bordo del tappo non viene impedito di scendere ulteriormente, quindi metti la sottile piastra di polistirolo, che espone la maggior parte del corpo dell'Ep tubo, nel bagnomaria bollente, e la sottile piastra di polistirolo galleggia naturalmente nel bagnomaria bollente. Il sottile foglio di polistirolo galleggia naturalmente sulla superficie dell'acqua bollente, facilitando l'accesso e il riscaldamento ed evitando spruzzi di acqua bollente.
Un lotto di provette Ep può essere posto nel bagnomaria bollente per tempi diversi. (Non gettare le provette Ep nel bagnomaria bollente, i coperchi potrebbero essere lavati via) e poi lasciarle raffreddare a temperatura ambiente per l'uso. Se il campione non viene utilizzato per un periodo di tempo più lungo, conservarlo in frigorifero a -20 gradi Celsius e, quando necessario, riscaldare il campione in acqua bollente a 110 gradi Celsius per 3 minuti a temperatura ambiente e raffreddarlo prima di rimuoverlo per l'uso e quindi applicare il campione per rimuovere gli aggregati substabili nelle proteine del campione.
(3) Cambiare la soluzione tampone del campione in modo che il campione possa essere completamente disciolto e la quantità di SDS sia sufficiente.
Motivo: le bande SDS sono legate elettroforeticamente alle proteine vicine. Oltre al sovracampionamento e alla dissoluzione incompleta del campione, la perdita dei pozzetti del gel può causare l'allargamento delle bande elettroforetiche. La perdita è spesso causata da crepe tra il gel e la lastra di vetro. Contromisure: in questo momento, il gel può solo essere preparato nuovamente, il pettine deve fare attenzione quando si solleva la coesione del gel, la velocità non deve essere troppo elevata, la direzione di sollevamento deve essere perpendicolare alla superficie del gel; per evitare crepe tra la lastra di vetro su entrambi i lati del gel e il gel, non comprimere la lastra di vetro su entrambi i lati del gel durante il processo di preparazione del gel.



